
동물실험금지가 전 세계 국가의 일반화한 규제로 자리잡고 있는 과정에서 안전성 예측 시스템의 중요성이 확산하고 있는 추세다. 그럼에도 불구하고 화장품 업계에서는 이러한 예측 시스템의 접근성에 대한 어려움을 호소하고 있는 실정이다. (재)대한화장품산업연구원(원장 이재란· www.kcii.re.kr ·이하 연구원)은 화장품 업계, 특히 중소 수출 중심 기업들의 이같은 난제 해결을 지원하기 위한 교육 프로그램을 기획, 내달 2일과 3일 이틀에 걸쳐 ‘화장품 원료 안전성 예측 시스템 교육’(무역센터 중회의실)을 연다고 밝혔다. 연구원 측은 “원료 안전성 예측 시스템 관련 교육을 통해 화장품 원료가 인체에 미치는 영향을 사전에 확인하기 위한 다양한 대체 시험법을 소개하는 한편 각 시험법을 안전성 평가에 어떻게 적용할 수 있는지 등 전문가들의 강연을 통해 지식과 정보를 공유할 예정”이라고 설명했다. 화장품 원료 안전성 예측 시스템은 동물실험을 금지·제한하고 있는 화장품 산업에서 화장품 성분에 대한 안전성을 예측할 수 있는 대체 시험법으로 대두되고 있는 상황. 그렇지만 실제로 예측 시스템을 사용하는데 있어 사용방법과 활용 사례 등 접근이 어려운 부분도 존재한다. 연구원은

미국 화장품 규제 현대화법(이하 MoCRA) 연말 시행을 앞두고 국내 화장품 업계의 긴장감이 높아지고 있는 가운데 대한화장품협회(회장 서경배· www.kcia.or.kr )가 미국뿐만 아니라 유럽·아세안·호주·캐나다 등 주요 해외 국가의 자외선차단제 관련 규정을 살펴볼 수 있는 웨비나를 연다. 화장품협회는 “오는 19일(목) 오후 4시 30분부터 ‘자외선차단제 주요국 제도 비교에 대한 웨비나’를 개최할 예정”이라고 공식 확인했다. 연자는 글로벌 규제관련 컨설팅 기업 Browne&Associates Consulting Ltd.에서 화장품·OTC 제품 관련 규정 컨설팅을 맡고 있는 산드라 M. 브라운(Sandra M. Browne) 씨다. 화장품협회는 “미국 자외선차단제 OTC 규정을 중심으로 유럽과 아세안·호주·캐나다 등 주요 국가의 자외선차단제 규정을 살필 예정이다. 영어-한국어 순차통역으로 진행하고 실시간 질의응답 시간도 준비했다”고 밝혔다. 참가신청은 화장품협회 홈페이지 공지사항 ‘자외선차단제 주요국 제도 비교에 대한 웨비나’ 게시글 클릭 후 사전등록 링크( https://forms.gle/eYDBNAPN8HMbpR2KA )를 통해 오는 10월 1
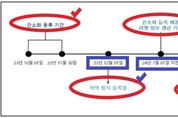
중국 정부가 화장품과는 별도로 치약에 대한 별도 규정을 마련, 시행에 들어간다. 중국 국가약품감독관리국(이하 NMPA)은 지난달 25일자로 ‘치약 감독관리조치’ 규범에 따라 치약 규제 요구사항과 현재 시판 중인 치약 등록 요건 간소화에 관한 사항을 발표했다. 이는 지난 3월 23일 중국 국가시장관리감독총국(이하 SAMR)이 발표한 ‘치약감독관리방법’에 대해 구체화한 제품 등록에 관한 내용을 담고 있다. 이에 따라 중국 시장에 판매할 치약 제품은 오는 12월 1일부터 ‘치약등록 정보서비스 플랫폼’을 통해 등록 진행을 필수화하고 간소화 등록 요건 등의 내용을 숙지해야 할 필요가 생겼다. 해당 규정의 주요 내용은 △ 중국으로 수출하는 치약 제품들은 올해 12월 1일부터 제품 출시 이전에 치약등록 정보서비스 플랫폼을 통해 등록을 반드시 진행해야 하고 △ 제품 등록 시 제품 효능에 대한 근거자료 개요도 함께 제출이 요구하되 ‘청결’ 효능만 클레임하는 제품은 효능 근거자료 개요 제출을 면제한다는 것 등이다. 해당 플랫폼은 지난달 22일부터 가동하기 시작했다. 이와 함께 12세 이하의 어린이가 사용하는 어린이 치약에 관한 내용도 포함하고 있다. 즉 어린이용 치약은 ‘청결

중국 정부의 화장품 원료 안전 정보 등록 규정이 한층 강화돼 시행에 들어갔다. 이에 따라 중국 화장품 원료 등록과 관련한 우리나라 기업의 대응 역시 또 다른 장벽을 뚫어야 할 상황에 놓일 가능성이 높아지고 있다. 관련 업계에 따르면 중국 국가약품감독관리국(이하 NMPA)은 산하 기관 식약품검정연구원(이하 NIFDC)을 통해 화장품 원료 안전 정보 등록 플랫폼 운영 방침을 개정했으며 특히 원료 안전 정보 등록의 경우 기존 ‘단일·복합 조성 원료 모두 등록 가능’에서 ‘단일 조성 원료만 등록 가능’으로 변경하는 등 국내 기업의 대응이 한층 까다로워질 가능성이 짙어지고 있다는 것. 등록 플랫폼의 주요 업데이트 내용을 살펴보면 우선 중국 화장품 기 사용 원료 목록에 명기한 순번을 입력할 수 있도록 추가했다. 이에 따라 등록 하고자 하는 원료의 기 사용 목록의 순번을 입력하면 자동으로 해당 하는 성분명에 대한 조회가 가능하다. 두 번째는 단일 조성 원료만 등록이 가능하도록 시스템을 변경했다. 이에 더해 기존 복합원료 조성비 입력란 역시 두 개 이상의 성분을 입력할 수 없도록 변경함으로써 복합 원료의 안전 정보 등록이 불가능해졌다. 이전까지 복합 원료를 등록하면서 기재

식품의약품안전처(처장 오유경· www.mfds.go.kr )가 인체 유래 세포 배양액(인체에서 유래한 세포를 배양한 후 세포를 제거하고 남은 액)을 원료로 사용하는 화장품을 유통·판매하는 책임판매업체(생산실적 상위 36곳·점유율 75%)를 현장 점검한 결과 ‘화장품법’에 따른 안전기준 자료의 작성·보존 의무를 이행하지 않은 3곳을 적발, 관할 지방식약청에 행정처분을 요청했다고 밝혔다. 해당 화장품법 관련 △ 1차 위반 시에는 판매업무 정지 3개월 △ 2차 위반 시 정지 6개월 △ 3차 위반 시 정지 12개월 △ 4차 이상 위반 적발 시에는 책임판매업 등록을 취소할 수 있다. 식약처는 관련해 “인체 유래 세포 배양액은 식약처에서 고시한 안전기준(‘화장품 안전기준 등에 관한 규정’ [별표 3] 인체 세포·조직 배양액 안전기준)에 적합한 경우에만 사용할 수 있다”고 전제하고 “인체 유래 세포 배양액이 들어있는 화장품의 책임판매업체는 △ 공여자의 적격성 검사 자료 △ 인체 세포의 채취·검사기록서와 배양기록서 △ 독성시험자료 등 안전기준에서 정한 모든 기록과 성적서 등을 완제품 제조일로부터 3년까지 보존해야 한다”고 이번 점검 결과에 대한 배경과 기준을 제시했다. 이

식품의약품안전처(처장 오유경· www.mfds.go.kr )가 화장품·식품·의약(외)품 등의 수출 확대를 위해 수출지원 정책 기능을 전담하는 식약처장 직속 ‘글로벌수출전략담당관’을 신설, 출범했다. 새롭게 출범한 식약처 글로벌수출전략담당관은 우수한 국산 화장품·식품·의료제품의 글로벌 시장 진출을 뒷받침하기 위해 과학적 근거에 기반, △ 국산 화장품·식의약 제품의 글로벌 위상 제고 △ 주요 수출 대상국 규제 장벽을 해소하기 위한 규제기관 간 협력(R2R: Regulatory authority to Regulatory authority) 추진 △ 글로벌 경쟁력 확보 위한 수출지원 체계를 구축 등의 수출 전략을 수립·추진한다. 식약처는 지난해 8월 말부터 ‘글로벌 식의약정책 전략추진단’(이하 추진단)을 선제 운영해 왔다. 추진단은 그 동안 중국의 수입 화장품 원료 정보 요구 등과 같이 강력한 규제 적용을 통한 진입 장벽을 높이는 상황에서 규제기관 간 협력 등을 통해 수출을 지원하는 등의 활동을 전개했다. 특히 1년간 추진단을 운영하면서 △ 아시아-태평양 식품 규제기관장 협의체(APFRAS(아프라스): Asia-Pacific Food Regulatory Author

잘못된 사용법과 오류가 있는 제품 지식 등으로 인해 발생할 수 있는 소비자 피해를 막기 위한 소비자 교육 프로그램이 식품의약품안전처·국립창원대학교·(사)미래소비자행동 등 관·학·민 공동 참여로 가동에 들어간다. 식품의약품안전처(처장 오유경· www.mfds.go.kr )는 “영유아 화장품과 두발용 화장품(퍼머넌트 웨이브·헤어 스트레이트너·염모제·새치커버 샴푸) 등에 대한 올바른 사용 방법을 안내해 잘못된 지식과 사용으로 인한 소비자 피해를 예방한다는 목표로 △ 화장품 종류별 선택 기준 △ 올바른 사용 방법 △ 사용 시 주의사항 등을 설명하는 교육을 내달 1일부터 20일까지 진행한다”고 밝혔다. 특히 이번 교육 프로그램 대상 품목으로 설정한 영유아·두발용 화장품은 최근 3년(2020년~2022년) 동안 보고가 이뤄진 유해사례 등 안전성 정보를 분석한 결과 생산실적 대비 안전성 보고 비율이 높았던 제품이라는 점에서 이번 교육의 필요성과 가치가 높다. 교육을 원하는 기관·단체의 경우 오는 13일(금)까지 신청하면 맞춤형으로 시간·장소를 정해 대면으로 진행하고 개인 자격은 같은 일정(13일)까지 사전 신청자들을 대상으로 온라인 교육을 실시한다. 이번 교육에 활용하는

식품의약품안전처가 K-뷰티 글로벌화를 위한 다양한 방안을 산업 현장의 현실과 요구를 반영한 규제혁신을 통해 추진하겠다는 의지를 거듭 확인하고 있다. 오유경 식품의약품안전처장은 지난 22일 식약처가 전개하고 있는 화장품 분야 규제혁신이 현장에서 정착할 수 있도록 맞춤형화장품 판매장(아모레성수·서울 성동구 소재)을 방문, 현장의 목소리를 듣고 맞춤형화장품 제조와 관련한 전 과정을 직접 경험했다. 식약처 공식 발표에 의하면 오유경 처장은 이날 “화장품 업계의 끊임없는 기술개발과 혁신 노력, 그리고 정부 지원을 통해 K-뷰티가 전 세계에서 사랑받는 대표 한류 브랜드가 됐다”며 “특히 지난해 많은 어려움 속에서도 △ 화장품 세계 4위 수출국 △ 2년 연속 10조 원 수출실적을 달성했다”고 격려한 것으로 전해졌다. 이와 함께 오 처장은 화장품 산업 지속 발전 지원을 위해 혁신 규제 발굴과 개선을 지속해 왔다는 점을 들고 “마스크를 벗으면서 올해 들어 립스틱 1억2천만 개 수출실적을 올리는 등 색조화장품의 위상과 인지도 역시 높아지고 있으며 식약처가 규제혁신2.0(48번 과제)을 통해 개선한 색소 품질관리 방법(‘화장품의 색소 종류와 기준·시험방법’·2023년 9월 21

추석 명절을 앞둔 시점에서 소비자들의 선호도가 높은 △ 미백·주름 기능성화장품 △ 보디워시·스크럽 제품 등에 대한 광고물을 점검한 결과 53건에 이르는 부당광고가 적발됐다. 식품의약품안전처(처장 오유경· www.mfds.go.kr )가 지난달 28일부터 이달 8일까지 온라인 광고 게시물을 집중 점검한 결과 화장품과 식품·의료기기·의약외품 등의 허위·과대광고 총 509건을 적발한 것으로 드러났다. 식약처는 이와 관련해 “이들 위반 광고에 대해서는 방송통신심의위원회 등에 신속하게 접속 차단을 요청하는 한편 특히 반복 위반 업체는 관할 행정기관에 행정처분 등을 의뢰했다”고 오늘(21일) 공식 발표했다. 식약처 발표에 의하면 화장품의 경우 선물로 선호도가 높은 △ 미백·주름 기능성화장품 △ 보디워시 △ 보디스크럽 제품 등에 대한 광고 게시물을 점검한 결과 부당광고 53건이 적발됐다는 것. 적발한 화장품 광고의 주요 위반 유형은 △ 화장품이 의약품의 효능·효과가 있는 것처럼 광고 33건(62%) △ 일반화장품을 기능성화장품처럼 광고하거나 기능성화장품으로 심사받은 결과와 다른 내용으로 광고 19건(36%) △ 화장품의 범위를 벗어나 소비자가 오인할 우려가 있는 광고 1

올해 연말 발효를 앞두고 있는 미국 ‘화장품 규제 현대화법’(The Modernization of Cosmetics Regulation Act of 2022· 이하 MoCRA)과 관련해 이어지고 있는 미국 FDA의 후속조치의 강도가 예상을 넘어서는 수준에 이르고 있다. 미국 FDA가 지난 15일자로 발표한 ‘Draft Cosmetics Direct Electronic Submissions Portal’이라는 제목의 문서에는 화장품 제조기업과 브랜드사가 MoCRA 서류 제출 시스템 오픈 이전에 세부 내용을 꼼꼼하게 확인해야 할 규정(조항)들이 곳곳에 존재하고 있다는 것이다. <파일 원문 바로가기: https://www.fda.gov/media/171557/download?attachment > 지난 두 차례에 걸쳐 MoCRA 시행과 관련한 기고문을 게재한 바 있는 홍정훈 리소스오브케이뷰티 대표는 “FDA가 발표한 가장 최근(9월 15일) 문서에서 지금까지 확인해 왔던 주요 방침들보다 강화한 내용들을 발견했고 이는 국내 화장품 기업들에게 당초의 예상을 뛰어넘는 영향을 미칠 가능성이 높다”고 지적했다. 우선 제조기업(Facility) 등록시 시설에서 제

(재)대한화장품산업연구원(원장 이재란· www.kcii.re.kr ·이하 연구원)이 올해 두 번째 ‘화장품 안전성 평가 전문인력 양성 교육 프로그램’을 내달 26일부터 가동한다. 연구원은 보건복지부 지원을 통해 주요 국가별 화장품 안전관리 기준을 준수해 안전한 화장품의 수출을 촉진하기 위한 취지로 지난 7월 제 1차 안전성 평가 전문인력 양성 교육에 이어 두 번째 교육 프로그램을 시행하는 것. 연구원 관계자는 “지난 1차 교육 피드백을 바탕으로 ‘실무에 도움이 되는 교육’을 목표로 설정해 오는 10월 26일부터 2차 교육에 들어간다”고 확인했다. 10월 31일(화)일까지 모두 4일에 걸쳐 23시간 교육이 이뤄진다. 화장품 안전성 평가 업무를 수행하거나 이에 관심이 있는 화장품 관련 종사자를 대상으로 소규모(선착순 30명)로 진행할 예정이다. 특히 이번 2차 교육에서는 독성학자 Vera Rogiers 교수를 초청해 별도의 교육 프로그램을 마련했다. Vera Rogiers 교수는 현재 EU 소비자안전과학위원회(SCCS) 부의장을 맡고 있으며 유럽 화장품 안전성 평가 교육 프로그램 운영 책임과 함께 직접 강의하고 있다. 이번 교육에서 △ EU 규제(EC) N°12

미국 ‘화장품 규제 현대화법’(The Modernization of Cosmetics Regulation Act of 2022· 이하 MoCRA)의 연말 발효를 앞두고 국내 화장품 업계 발등에 불이 떨어졌다. 연초부터 MoCRA 제정과 발효, 진행 과정 등 일련의 내용들을 지속 업데이트해 온 코스모닝은 해당 법 시행 약 4개월 여를 앞둔 현 시점에서 가장 유의해야 할 사안들을 점검하고 이에 대한 적절한 대책 마련을 위해 홍정훈 리소스오브케이뷰티(ROK) 대표의 기고문을 입수, 게재한다. 홍 대표는 MoCRA 관련 전체 내용을 포함해 우리나라 화장품 기업이 수립해야 할 대안 등에 대해 코스모닝닷컴에 기고한 바 있으며 지난 8월 17일 대한화장품협회가 주관·주최한 30차 CEO 조찬간담회를 통해 국내 화장품 업계의 대응 방향을 제시했다. 이번 기고문은 조찬간담회에서 제기됐던 일부 의문 사항과 이후 변경 내용, 그리고 해석의 차이에 따라 논란의 여지가 있는 부분들을 다시 확인해 독자 여러분께 전한다. 이와 함께 홍 대표의 기고문이 MoCRA 관련 모든 사안에 대한 ‘정답’이 될 수는 없으며 국내 타 관련 기관과 미국 FDA(관계자)의 견해·법(조항) 해석 등에 의