기능성화장품 심사 규정 개정(안) 행정예고

탈모 증상 완화에 도움을 주는 기능성화장품 가운데 △ 복합제로서 덱스판테놀 0.2%·살리실릭애씨드 0.25%·엘-멘톨 0.3 % △ 복합제로서 나이아신아마이드 0.3%·덱스판테놀 0.5%·비오틴 0.06%·징크피리치온액(50%) 2.0%의 조합을 사용할 경우에는 안전성·유효성 자료 제출을 하지 않아도 무방하다.
또 지난 8월 개정한 화장품법 시행규칙에 의해 기능성화장품에서 ‘아토피’ 표현이 삭제됨으로써 이에 대한 인체적용시험은 일반화장품과 동일한 시험기관에서 할 수 있게 됐다.
식품의약품안전처(처장 이의경· www.mfds.go.kr )는 이 같은 내용을 골자로 한 ‘기능성화장품 심사에 관한 규정’ 개정(안)을 행정예고했다.
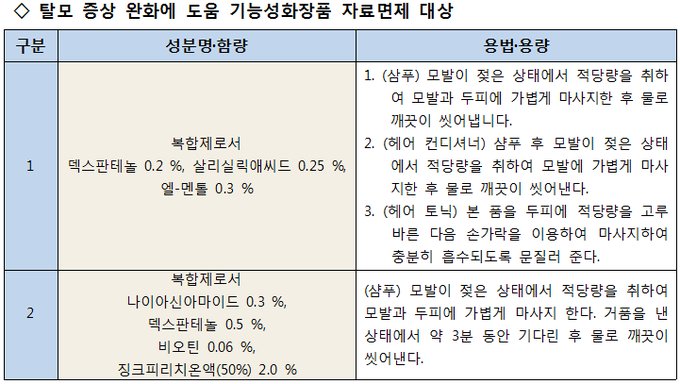
이에 따라 탈모 증상 완화에 도움을 주는 기능성화장품 가운데 고시한 성분·함량 조합(복합제로서 덱스판테놀 0.2%·살리실릭애씨드 0.25%·엘-멘톨 0.3 %/ 복합제로서 나이아신아마이드 0.3%·덱스판테놀 0.5%·비오틴 0.06%·징크피리치온액(50%) 2.0%)을 사용할 경우에는 기능성화장품 심사 시 안전·유효성에 관한 자료 제출을 면제토록 했다.
화장품법 시행규칙 개정(2020년 8월)으로 기능성화장품에서 아토피 표현이 삭제됨에 따라 해당 제품(피부장벽의 기능을 회복해 가려움 등의 개선에 도움을 주는 화장품)에 대한 인체적용시험을 일반화장품 시험기관에서도 수행할 수 있다.
즉 이전에는 의약품 임상시험실시기관에서만 가능했었지만 ‘국내외 대학 또는 화장품 관련 전문 연구기관 등’으로 그 범위 확대가 이뤄진 것이다.
식약처 관계자는 “이번 개정 추진으로 기능성화장품의 개발의 활성화와 빠른 시장 진입이 가능할 것으로 기대한다”고 밝혔다.










































