미국 FDA의 ‘OTC 모노그래프 드럭’과 관련한 새로운 규정 적용방침이 발표됨에 따라 미국 수출을 위한 OTC 제품(자외선차단제·불소치약·가글·비듬샴푸·여드름화장품)을 제조하는 기업의 경우 FDA 등록비로 매년 1만3천548달러에서 최고 2만322달러(한화 약 1천511만 원~2천267만 원)의 비용을 부담해야 할 상황에 직면했다.
미 FDA의 이 같은 ‘사용자 비용 프로그램’(User Fee Program) 실시에 따라 관련 품목 제조업체는 오는 5월 9일까지 등록을 완료해야 하며 유효기간은 소급 적용돼 ‘2020년 10월 1일부터 2021년 9월 30일’까지다.
특히 5월 10일까지 등록과 함께 비용 지불을 완료하지 않은 기업은 미 FDA로부터 청구서(Invoice)을 받게 된다. 관련 청구서를 받은 날로부터 20일 이내에 해당 비용을 지불하지 않을 경우 체납목록에 등록, 공개하고 해당 시설에서 생산되는 모든 OTC monograph 품목(해당 시설에서 제조된 성분을 포함하는)을 ‘Section 502(ff)’에 따라 ‘미등록제품’(misbranded)으로 간주할 예정이라는 것.
관련해 국내 화장품 업계, 특히 미국 수출을 위한 제품을 제조하는 기업은 해당 품목을 수출하기 위해서 매년 1천500만 원 이상의 등록비 부담을 피할 수가 없게 된 상황이다.
미국 수출업무를 진행하고 있는 한 관계자는 “미 FDA의 이번 규정 시행이 국내 화장품 업계에도 영향을 미치게 되는 것은 등록과정에서 매년 발생하는 비용 부담과 함께 해당 OTC품목에 대해서는 미 FDA의 관리 아래 놓이게 될 가능성이 커졌다는 점”이라고 지적하고 “등록을 하지 않게 되면 ‘미등록제품’으로 분류되고 등록을 하게 되면 비용과 함께 미 FDA가 상시 감사(Audit)를 할 수 있는 상황에 놓이기 때문”이라고 현 상황에 대한 우려를 표명했다.
OTC 모노그래프 퍼실러티 유저 비용(Monograph Facility User Fee)
미 FDA의 관련 규정 시행은 지난해로 거슬러 올라간다. 지난해 3월 27일 도날드 트럼프 당시 대통령은 ‘코로나 바이러스 원조·구호·경제 안보법’(이하 CARES Act)에 서명했고 이후 FDA는 CARES Act에 근거, OTC 모노그래프 드럭에 대한 새로운 규정을 발표한다.
이 사용자 비용 프로그램 규정은 지난해 12월 29일 처음 발표됐으나 미 FDA의 내부 사정으로 올해 1월 6일 철회가 이뤄졌다. 그렇지만 이 규정을 지난 3월 26일 ‘FY(회계년도)2021’을 위해 최종 확정, 발표한 것이다.
다만 미 FDA 측은 △ 2019년 12월 31일 이전 OTC 모노그래프 드럭 활동을 중단하고 이를 등록에 반영한 경우 △ 2019 코로나19 대유행 기간 동안 FDA에 등록한 기관으로 2020년 1월 27일 이후 OTC 손소독제(OTC Hand Sanitizer Products) 제품을 제조하는 것으로 등록된 회사는 비용의 면제대상이 된다고 예외 규정도 명시했다.
미 FDA 측은 “새로운 규정을 통해 FDA가 규제활동을 적시에 수행하고 혁신성있는 OTC 모노그래프 드럭에 대한 업무 수행을 하는데 도움이 될 것으로 예상한다”고 밝혔지만 정작 해당 품목을 미국으로 수출해야 하는 국가에 대해서는 일종의 ‘비관세 무역장벽’에 다름 아니라는 시각이 우세하다.
자외선차단제품 등 제조기업, 매년 1500만 원 이상 등록비 소요
미 FDA의 새 규정 시행에 따라 OTC 품목으로 분류하는 ‘자외선차단제품·불소치약·가글·비듬샴푸·여드름 케어 관련 화장품 제조기업은 사용자 비용 프로그램에 의해 납부 대상에 해당한다.
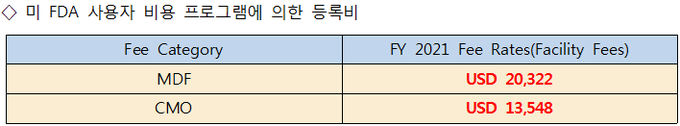
다만 해당 품목이 OTC 모노그래프 드럭을 이용해 등록된 OTC 품목인지는 확인해야 한다. 만일 제조사에서 손소독제 이외에 다른 OTC 품목을 제조할 경우에는 등록과 비용이 소요된다.
OTC 품목 책임판매업자(브랜드 오너)는 사용자 비용 프로그램의 부과 대상이 아니지만 해당 제품 제조기업이 사용자 비용을 지불하고 등록을 해야만 합법성에 근거한 미국 수출이 가능하다는 점에서 반드시 이번 새 규정을 확인해야 한다.
■ 용어 해설
△ OTC 모노그래프 드럭(OTC Monograph Drug): 신약신청이 없는 비처방 의약품.
△ OTC 모노그래프 드럭 퍼실러티(OTC Monograph Drug Facility·MDF): OTC 모노그래프 드럭의 완제품을 제조하거나 처리하는데 관여하는 국내 혹은 외국 회사
△ Contract Manufacturing Organization(CMO): 소유주 혹은 소유주 시설의 계열사가 그 공장에서 직접 생산한 OTC 모노그래프 드럭을 미국의 도·소매업체 또는 소비자에게 직접 판매하지 않는 의약품 제조업체
△ OTC 모노그래프 오더 리퀘스트(OTC Monograph Order Request·OMOR): 제출된 OTC 모노그래프 드럭에 대한 행정명령요청(신규요청)









































